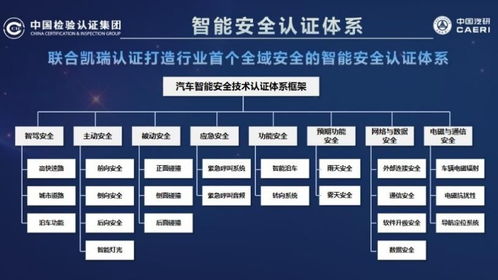
近日,中國汽車工程研究院(簡稱“中國汽研”)正式發布了行業首個全域智能安全技術認證體系,這一舉措標志著汽車行業在計算機軟硬件技術開發領域邁出了關鍵一步。該體系旨在通過系統性認證,提升智能汽車在感知、決策、執行等環節的安全性,為行業提供統一的技術標準和測試規范。隨著汽車智能化水平的不斷提升,計算機軟硬件技術成為智能安全的核心驅動力。中國汽研的全域認證體系覆蓋了硬件可靠性、軟件算法魯棒性、數據安全與隱私保護等多個維度,確保車輛在復雜場景下的穩定運行。這不僅有助于車企優化產品設計,降低安全風險,還將推動產業鏈上下游的技術協同與創新。未來,該認證體系有望為全球智能汽車發展提供參考,加速計算機軟硬件技術在汽車安全領域的深度應用。
中國汽研發布行業首個全域智能安全技術認證體系 推動計算機軟硬件技術開發新標準
如若轉載,請注明出處:http://www.qs7k4.cn/product/9.html
更新時間:2026-06-03 16:28:15
產品列表
PRODUCT
----------------